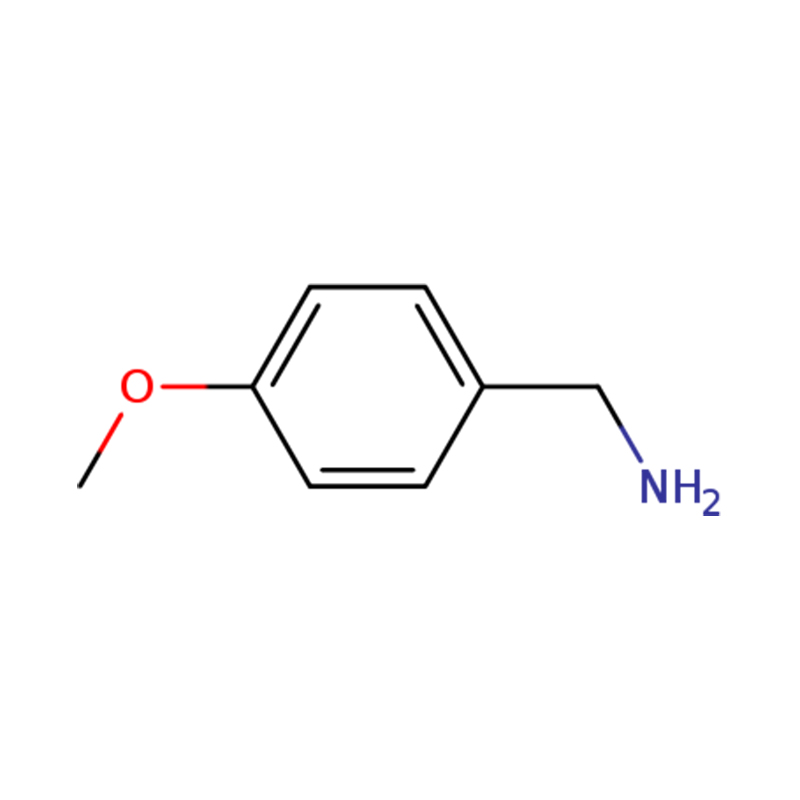
1-(4-เมทอกซีฟีนิล)เมธานามีน
รายละเอียดสินค้า
| แคสโน | 2393-23-9 | เวลาจัดส่ง | ภายใน 10 วัน |
| โมเลกุล | C8H11NO | กำลังการผลิต | 1 เมตริกตัน/วัน |
| รูปร่าง | ของเหลวใสไม่มีสีจนถึงสีเหลืองเล็กน้อย | ความบริสุทธิ์ | 99% นาที |
| แอปพลิเคชัน | สารตั้งต้นทางเภสัชกรรม | พื้นที่จัดเก็บ | อุณหภูมิห้อง มืด ปิดสนิท |
| หมายเลขจำกัด | 1 กิโลกรัม | การขนส่ง | ทางอากาศ,ทางทะเล,ด่วน |
| ความหนาแน่น | 1.05g/mLat25°C(สว่าง) | จุดเดือด | 236-237°C(สว่าง) |
| จุดหลอมละลาย | -10 องศาเซลเซียส | ดัชนีหักเหแสง | n20/D1.546(ตามตัวอักษร) |
| จุดวาบไฟ: | >230°ฟาเรนไฮต์ | ความสามารถในการละลาย | ละลายน้ำได้สูง |
| ชื่อ | พี-อะนิซิลามีน หรือ (4-เมทอกซีฟีนิล)เมทานามีน |
คำพ้องความหมาย
LABOTEST-BB LTBB000703; AKOS BBS-00003589; 4-AMINOMETHYL-ANISOLE; 4-METHOXYBENZYLAMINE; P-Methoxybenzylamine Hydrochloride173.64; 4-Methoxybenzylamine, 98+%; สำหรับ Sparfloxacine; P-METHOXYBENZYLAMINE HYDROCHLORIDE
แอปพลิเคชัน
สามารถใช้สำหรับการสังเคราะห์สารตั้งต้นทางเภสัชกรรม เป็นอันตรายต่อน้ำเล็กน้อย ห้ามให้ผลิตภัณฑ์ที่ไม่ได้เจือจางหรือปริมาณมากสัมผัสกับน้ำใต้ดิน ทางน้ำ หรือระบบบำบัดน้ำเสีย หากไม่ได้รับอนุญาตจากรัฐบาล ห้ามปล่อยสารลงสู่สิ่งแวดล้อมโดยรอบ เพื่อหลีกเลี่ยงการสัมผัสออกไซด์ กรด อากาศ และคาร์บอนไดออกไซด์ ควรปิดภาชนะบรรจุให้สนิท เก็บไว้ในที่แห้งและเย็น
ห้องปฏิบัติการ QC
มีห้องปฏิบัติการควบคุมคุณภาพเฉพาะอยู่ภายในพื้นที่ ซึ่งดำเนินการทดสอบทางเคมี กายภาพ จุลินทรีย์ การศึกษาความคงตัว และการทดสอบเครื่องมือ เช่น IR, UV, HPLC, GC สำหรับวัตถุดิบและผลิตภัณฑ์สำเร็จรูป พื้นที่ทั้งหมดได้รับการควบคุมการเข้าถึงและบำรุงรักษาอย่างดี พร้อมด้วยเครื่องมือวิเคราะห์ที่เพียงพอสำหรับการทดสอบตามวัตถุประสงค์ เครื่องมือทั้งหมดได้รับการติดฉลากอย่างถูกต้องและผ่านการสอบเทียบอย่างถูกต้อง
QA
QA มีหน้าที่ประเมินและจัดประเภทความเบี่ยงเบนออกเป็นระดับหลัก ระดับทั่วไป และระดับรอง สำหรับความเบี่ยงเบนทุกระดับ จำเป็นต้องมีการตรวจสอบเพื่อระบุสาเหตุหลักหรือสาเหตุที่อาจเกิดขึ้น การตรวจสอบต้องเสร็จสิ้นภายใน 7 วันทำการ การประเมินผลกระทบต่อผลิตภัณฑ์พร้อมกับแผน CAPA จะต้องดำเนินการหลังจากการตรวจสอบเสร็จสิ้นและระบุสาเหตุหลักแล้ว ความเบี่ยงเบนจะถูกปิดลงเมื่อนำ CAPA ไปใช้ ความเบี่ยงเบนทุกระดับจะต้องได้รับการอนุมัติจากผู้จัดการ QA หลังจากนำไปใช้แล้ว ประสิทธิภาพของ CAPA จะได้รับการยืนยันตามแผน